Perbedaan antara asam amino, peptida, dan protein adalah sebagai berikut:
- Asam Amino: tidak memiliki ikatan peptida
- Peptida: memiliki ikatan peptida
- Protein: merupakan polimer dari asam amino dengan jumlah lebih dari 50
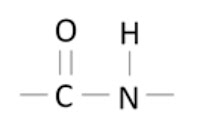
yang dimaksud dengan ikatan peptida adalah:
contoh asam amino yang paling sederhana:
 |
| Glisin |
 |
| dipeptida |
Salah satu contoh protein:
 |
| hemoglobin |
Asam amino essensial terdiri dari 10 asam amino, sebagai berikut:
 |
| 1. Fenilalanin (Phe), F |
 | ||
| 2. Triptofan (Trp), W |
 | |
| 3. Isoleusin (Ile), I |
 | |
| 4. Leusin (Leu), L |
 |
| 5. Lisin (Lys), K |
 | |
| 6. Metionin (Met), M |
 |
| 7. Treonin (Thr), T |
 | |
| 8. Valin (Val), V |
 | ||
| 9. Arginin (Arg), R |
 |
| 10. Histidin (His), H |
Sedangkan asam amino nonessensial terdiri dari 10 asam amino, sebagai berikut:
 | |
| 1. Asam Glutamat (Glu) |
 | |
| 2. Glutamin (Gln) |
 | |
| 3. Glisin (Gly) |
 |
| 4. Asam Aspartat (Asp) |
 | |
| 5. Asparagin (Asn) |
 |
| 6. Alanin (Ala) |
 | |
| 7. Prolin (Pro) |
 | |
| 8. Serin (Ser) |
 | |
| 9. Tirosin (Tyr) |
 |
| 10. Sistein (Cys) |
Setelah mengetahui struktur keduapuluh asam amino tersebut, maka di antaranya ada yang bersifat asam, basa, dan netral. Yang bersifat asam adalah asam glutamat dan asam aspartat, yang bersifat basa adalah lisin, arginin, dan histidin, sedangkan sisanya bersifat netral.
Suatu asam amino mengalami reaksi asam-basa internal sehingga membentuk suatu ion dipolar, atau disebut juga sebagai zwitterion.
Sebagai tambahan, pKa dalam asam amino bukanlah dilihat dari adanya gugus -COOH, melainkan karena adanya gugus NH3+. Dan pKb dalam asam amino bukan pula dilihat dari adanya gugus -NH2, melainkan dari adanya gugus -COO-.
Oleh karena itu, asam amino yang di dalam larutannya membentuk zwitterion, apabila berada dalam laruatn asam, maka asam amino akan bersifat asam.
Sedangkan apabila asam amino berada dalam larutan basa, maka asam amino akan bersifat basa.
Cara memisahkan suatu jenis asam amino dari campuran beberapa asam amino dapat menggunakan prinsip elektroforesis. Suatu asam amino yang memiliki muatan positif akan tertarik menuju katoda, dan muatan negatif akan tertarik ke anoda, sedangkan muatan netral akan diam di tempat.
Misalkan suatu campuran terdiri dari asam aspartat, lisin, dan glisin, maka cara memisahkan glisin dari campuran adalah dengan cara elektroforesis, sudah kita ketahui bahwa lisin merupakan asam amino yang bersifat basa, dan dalam larutannya lisin akan terionkan dan akan lebih bermuatan positif sehingga tertarik menuju katoda, dan kita juga sudah mengetahui bahwa asam aspartat bersifat asam, dan dalam larutannya lebih bermuatan negatif sehingga akan bergerak menuju anoda. Dan glisin sebagai asam amino netral, akan terionkan dalam bentuk zwitterion, sehingga tetap diam di tempat, sehingga dalam larutan hanya terdapat glisin saja, begitulah caranya memisahkan glisin dari campuran tersebut.
Untuk mensintesis suatu asam amino dapat pula dilakukan dengan sintesa-sintesa berikut:
1. Sintesa Strecker, Sintesa ini terdiri dari dua tahap. Tahap pertama yaitu mereaksikan suatu aldehida dengan NH3, kemudian mengeluarkan H2O, setelah itu mereaksikannya dengan HCN, sehingga terbentuklah suatu aminonitril. Pada tahap kedua inilah terbentuk asam amino, dari hidrolisis aminonitril yang sebelumnya.
2. Biosintesa reduksi aminasi asam (alfa)-keto. Dengan melakukan reaksi aminasi terhadap suatu asam (alfa)-keto, kemudian mereduksinya dengan NaBH4.
Tentunya untuk mensintesis suatu asam amino tidak hanya melalui kedua reaksi tersebut di atas, dapat pula melalui reaksi-reaksi lainnya, seperti sintesa amidomalonat dan lain sebagainya. Namun saya kurang memahami reaksi-reaksi lainnya tersebut. Saya mohon maaf atas kekurangannya :(
Karena di perkuliahan saya, kimia organik hanya dipelajari dalam 3 sks, menurut saya kebanyakan dari teman-teman saya termasuk saya sendiri, lebih mengandalkan catatan-catatan penting dan soal-soal sebelumnya yang pernah diberikan oleh dosen untuk angkatan-angkatan sebelumnya. Bisa dibilang kami "apal mati" tanpa mengetahui alasan mengapa bisa begini atau bisa begitu. Tentunya kami memiliki keinginan untuk mengetahui lebih mengenai hal tersebut, namun karena keterbatasan waktu dan dikejar kurikulum, kami tidak bisa berbuat lebih, selain "apal mati".
Jawaban:
Suatu asam amino mengalami reaksi asam-basa internal sehingga membentuk suatu ion dipolar, atau disebut juga sebagai zwitterion.
 |
| zwitterion |
Oleh karena itu, asam amino yang di dalam larutannya membentuk zwitterion, apabila berada dalam laruatn asam, maka asam amino akan bersifat asam.
 |
| asam amino dalam larutan asam |
 |
| asam amino dalam larutan basa |
Misalkan suatu campuran terdiri dari asam aspartat, lisin, dan glisin, maka cara memisahkan glisin dari campuran adalah dengan cara elektroforesis, sudah kita ketahui bahwa lisin merupakan asam amino yang bersifat basa, dan dalam larutannya lisin akan terionkan dan akan lebih bermuatan positif sehingga tertarik menuju katoda, dan kita juga sudah mengetahui bahwa asam aspartat bersifat asam, dan dalam larutannya lebih bermuatan negatif sehingga akan bergerak menuju anoda. Dan glisin sebagai asam amino netral, akan terionkan dalam bentuk zwitterion, sehingga tetap diam di tempat, sehingga dalam larutan hanya terdapat glisin saja, begitulah caranya memisahkan glisin dari campuran tersebut.
Mensintesis Asam Amino
Untuk mensintesis asam amino dari asam karboksilat adalah dengan melakukan reaksi halogenasi terlebih dahulu dengan bantuan P dan H2O. Kemudian setelah itu mereaksikannya dengan NH3, reaksi tersebut disebut sebagai aminasi suatu asam (alfa)-halo. (Perlu digunakan NH3 berlebih untuk menetralkan asam dan mencegah terjadinya alkilasi berlebih. Berikut reaksinya: |
| asam propanoat disintesis membentuk alanin (suatu asam amino) |
1. Sintesa Strecker, Sintesa ini terdiri dari dua tahap. Tahap pertama yaitu mereaksikan suatu aldehida dengan NH3, kemudian mengeluarkan H2O, setelah itu mereaksikannya dengan HCN, sehingga terbentuklah suatu aminonitril. Pada tahap kedua inilah terbentuk asam amino, dari hidrolisis aminonitril yang sebelumnya.
 |
| Tahap 1 |
 |
| Tahap 2 |
Tentunya untuk mensintesis suatu asam amino tidak hanya melalui kedua reaksi tersebut di atas, dapat pula melalui reaksi-reaksi lainnya, seperti sintesa amidomalonat dan lain sebagainya. Namun saya kurang memahami reaksi-reaksi lainnya tersebut. Saya mohon maaf atas kekurangannya :(
Karena di perkuliahan saya, kimia organik hanya dipelajari dalam 3 sks, menurut saya kebanyakan dari teman-teman saya termasuk saya sendiri, lebih mengandalkan catatan-catatan penting dan soal-soal sebelumnya yang pernah diberikan oleh dosen untuk angkatan-angkatan sebelumnya. Bisa dibilang kami "apal mati" tanpa mengetahui alasan mengapa bisa begini atau bisa begitu. Tentunya kami memiliki keinginan untuk mengetahui lebih mengenai hal tersebut, namun karena keterbatasan waktu dan dikejar kurikulum, kami tidak bisa berbuat lebih, selain "apal mati".
Berikut adalah beberapa kumpulan soal mengenai asam amino, peptida, dan protein beserta dengan jawabannya:
1. Tentukan arah migrasi dan kecepatan migrasi untuk elektroforesis yang dilakukan pada pH 5,5; 5,7; 7,6 antara campuran glisin (6,0); Fenilalanin (5,5), serin (5,7).Jawaban:
Arah migrasi:
gly: katodaser: katoda
phe: tetap
Kecepatan mingrasi:
gly>ser>phe
Arah migrasi:
gly: katodaser: tetap
phe: anoda
Kecepatan migrasi:
gly>phe>serin
Arah migrasi:
gly: anodaser: anoda
phe: anoda
Kecepatan migrasi:
phe>ser>gly2. Urutkan heksapeptida Arg, Gly, Leu, Pro, jika prolin pada C terminal dan N terminal. Hidrolisis parsial diperoleh sebagai berikut: H-Gly-Pro-Arg-OH; H-Pro-Leu-Gly-OH; H-Arg-Pro-OH.
Jawaban:

3. Klasifikasikan protein berdasarkan komposisi, bentuk 3 dimensi, dan strukturnya.
Jawaban
a. Berdasarkan komposisinya, protein dibedakan menjadi:
Protein sederhana:
Protein yang hanya terdiri dari asam amino, contoh: serum albumin
Protein terkonjugasi:
Protein yang mengandung gugus atau senyawa lain selain asam amino, contoh:
- Glukoprotein, mengandung karbohidrat, contoh: (gamma)-Globulin, Interferon,
dan Karboksipeptidase
- Lipoprotein, mengandung lipid, contoh: plasma dan (beta)-Lipoprotein
- Nukleoprotein, mengandung asam nukleat, contoh: ribosomal protein dan
Tobacco Mozaic Virus
- Phospoprotein, mengandung ester fosfat, contoh: casein
- Metaloprotein, mengandung logam, contoh: Feritin, Vit B 12, dan Vit B 6
b. Berdasarkan bentuk 3 dimensinya, protein dibedakan menjadi:
Fibrous Protein (insoluble), contoh:
- Collagen: jaringan ikat, tendon
- Keratin: rambut, tanduk, kuku, dan kulit
- Elastin: pada jaringan ikat elastin
Granular protein (soluble), contoh:
- Insulin
- Albumin
- Myoglobulin
- Ribonuklease
- Lisozim
c. Berdasarkan strukturnya:
- primer
- sekunder
- tersier
- kuartener
4. Tuliskan tahapan reaksi yang digunakan, menggunakan kode 3 huruf dan hasil akhir menggunakan kode 1 huruf, dari Leusilalanina dan Alanilleusina.
Jawaban:
a. Leusilalanina
- Lindungi gugus amino leusina sebagai derivat BOC
- Lindungi gugus karboksil alanina sebagai estermetil
- Gabung kedua asam amino yang telah dilindungi menggunakan DCC
- Hilangkan gugus proteksi BOC dengan penambahan asam
- Hilangkan estermetil dengan hidrolisis basa
H-L-A-OH ---> Leusilalanina
b. Alainilleusina
- Lindungi gugus amino alanina sebagai derivat BOC
- Lindungi gugus karboksil leusina sebagai estermetil
- Gabung kedua asam amino yang telah dilindungi menggunakan DCC
- Hilangkan gugus proteksi BOC dengan penambahan asam
- Hilangkan estermetil dengan hidrolisis basa
H-A-L-OH ---> Alanilleusina
Demikianlah beberapa hal mengenai asam amino, peptida, dan protein yang bisa saya sampaikan. Kurang lebihnya mohon maaf, as we know that NOBODY'S PERFECT, kalau ada yang salah mungkin ada dari para pembaca yang bisa memperbaiki. Terima kasih sudah berkunjung :D
sumber:
FESSENDEN & FESSENDEN Kimia Organik EDISI KETIGA Jilid 2
dari buku ajar dosen kimia organik farmasi UI bu Nelly, tapi ada daftar pustakanya, yaitu dari:
Morrison & Boyd, Organic Chemistry, 4th edition
John Mc Murry, Organic Chemistry, 3rd edition
John Mc Murry, Organic Chemistry, 5th edition
beberapa soal juga didapat dari catatan kakak kelas, kak Utari, tapi kakak tersebut juga tentunya mendapatkan materinya dari buku ajar bu Nelly















Sgt bermanfaat, terimakasih :)
ReplyDeleteSama-sama. Untuk lebih lengkapnya bisa dibaca langsung di buku Fessenden & FESSENDEN Kimia Organik.
ReplyDeleteterimakasih banyak infonya :)untuk proses dan prosedur kerjanya ada gak kak??
ReplyDeleteSama-sama :D
ReplyDeleteWah belum ada nih Lintang, ehehe
assalamualaium kak, kak kalo cara pemisahan ke 20 asam amino meggunakan metode elektroforesa bagaimana? Makasi kak
ReplyDeleteHalo Lulut, elektroforesis merupakan teknik pemisahan yang didasarkan atas pergerakan ion dan medan listrik. Sementara pergerakan ion bergantung pada muatan dan massanya. Ion yang bermuatan positif akan bergerak ke elektroda negatif, sebaliknya yang bermuatan negatif bergerak ke elektroda positif, sementara yang netral akan diam, tidak ada pergerakan. Terkait dengan massanya, ion dengan massa yang paling kecil akan bergerak lebih cepat dibandingkan dengan yang massanya lebih besar. Dalam hal pemisahan asam amino, asam amino dapat bersifat netral, asam, atau basa bergantung dari pH larutan. Contoh, asam amino glisin. Glisin memiliki titik isoelektrik di sekitar pH 6,0. Pada pH larutan 6,0 glisin tidak bermuatan, sementara di pH di bawah 6,0 (lebih asam) glisin bermuatan positif sehingga bergerak menuju elektroda negatif. Pada pH lebih dari 6,0 glisin bermuatan negatif sehingga bergerak menuju elektroda positif. Jadi, untuk mengetahui pergerakan senyawa asam amino, perlu untuk mengetahui titik isoelektriknya.
ReplyDeleteKarena tiap asam amino memiliki titik isoelektriknya, maka prinsip pemisahannya adalah dengan menggunakan pelarut dengan pH yang sesuai. Misal ingin memisahkan glisin dengan sistein (5,0), maka gunakan larutan dengan pH yang sama dengan glisin, yaitu 6,0. Pada pH larutan tersebut, glisin tetap berada dalam larutan, sementara sistein menjadi bermuatan negatif sehingga bergerak ke elektroda positif. Ketika elektroforesis telah selesai, larutan dalam sampel sudah berisi glisin saja, karena sisteinnya sudah bergerak ke anoda meninggalkan larutan sampel. Selanjutnya untuk pemisahan 18 asam amino yang lainnya prinsipnya sama.
Makasih banyak kak
ReplyDeleteSama-sama :D
ReplyDeleteAssalamu'alaikum kak, saya mau nanya kak. Kira kira penyebab koagulasi kuning telur yang dicampur dengan madu asli itu apa ya kak? Apa ada hubungannya antara protein dengan zat asam dari madu? Jika iya, mengapa hal tersebut terjadi?
ReplyDeleteTerimakasih kak :)
Email : jahrakhairunisa22@gmail.com
Halo Zahra, salah satu penyebab utama suatu protein mengalami koagulasi adalah suhu. Pada kasus ini, protein dalam telur dapat mengalami koagulasi pada suhu tertentu. Bagian putihnya dapat mengalami koagulasi pada suhu antara 144-149 derajat Fahrenheit/62,2-65 derajat selsius), bagian kuningnya berkoagulasi pada suhu antara 149-158 derajat Fahrenheit/65-70 derajat selsius, atau secara keseluruhan protein dalam telur dapat berkoagulasi pada suhu antara 144-158 derajat Fahrenheit/62,2-70 derajat selsius. (referensi: http://www.aeb.org/food-manufacturers/eggs-product-overview/functional-properties/39-functional-properties/211-coagulation)
ReplyDeleteSaya setuju bahwa penambahan asam bisa menjadi salah satu penyebab terkoagulasinya protein dalam hal proteinnya tersusun dari asam amino yang bersifat basa sehingga terjadi reaksi antara senyawa asam amino yang bersifat basa dengan asamnya. Reaktivitas asam amino bersifat basa dapat dilihat pada link ini, lihat pada gambar "Reaction of Histidine" -->
http://bio.libretexts.org/Core/Biochemistry/Proteins/Structure_and_Properties_of_Amino_Acids/Chemical_Reactivity_of_Amino_Acid_Side_Chains
Menurut saya, kalau asam aminonya bersifat asam ditambah dengan asam, maka tidak akan terjadi reaksi karena sama-sama asam sehingga asam aminonya tetap berada dalam bentuk molekul yang stabil.
Telur mengandung asam amino esensial berupa histidin, isoleusin, leusin, lisin, metionin, fenilalanin, treonin, triptofan, dan valin, serta asam amino nonesensial berupa alanin, asam aspartat, dan glutamat. Arginin, sistein, prolin, serin, dan tirosin juga terdapat dalam telur. (Referensi: http://healthyeating.sfgate.com/amino-acids-contained-milk-eggs-3992.html; http://www.jbc.org/content/186/1/23.full.pdf).
Dengan demikian terdapat kemungkinan terjadinya reaksi antara telur dengan madu, karena arginin, histidin, dan lisin (asam amino bersifat basa) terkandung di dalam telur.
Senyawa asam yang dikandung dalam madu dapat berupa asam asetat, asam butanoat, asam format, asam sitrat, asam suksinat, asam laktat, asam malat (referensi: http://www.chm.bris.ac.uk/webprojects2001/loveridge/index-page3.html)
Sejauh ini, itu yang saya tahu. Tentu perlu dicari lebih lanjut terkait dengan penyebab terjadinya koagulasi pada telur dengan madu, apakah benar karena asamnya, atau ada penyebab lainnya. Sudah di email ya. Sukses belajarnya :D
Maaf kak, saya mau nanya lagi, kira kira dalam ikatan-ikatan asam amino yang bersifat asam dan basa pada kuning telur mengalami penggaraman, lalu apa ada hubungannya dengan pemberian zat asam atau basa dapat merusak ikatan tersebut sehingga menyebabkan koagulasi? Jika iya, mengapa hal tersebut terjadi kak? Lalu bagaimana prosesnya?
ReplyDeleteZahra, mungkin koagulasi bisa terjadi akibat peristiwa penggaraman tersebut, namun saya sendiri masih ragu. Sebaiknya kamu mencari lebih lanjut penjelasannya melalui literatur-literatur lain karena saya sendiri tidak begitu mengerti. Terima kasih.
ReplyDeleteassalamu'alaikum kak mau tanya saya ada tugas 22 asam amino yang memiliki isoelektrik yang berbeda maksutnya gimana ya kak trimakasih ^^
ReplyDeleteHalo unknown, waalaikumsalam, mungkin kamu diminta untuk mengidentifikasi pergerakan asam aminonya pada elektroda. Maaf ya baru balas.
ReplyDeleteHY ..slamat malam nurul. saya mau bertanya, jika ada suatu virus yang memuat 4 jenis asam amino esensial dalam satu tubu virus. dan virus tersebut sudah menginfeksi inangnya, adakah solusi terbaik yang dapat dilakukan untuk membunuh virus tersebut,,????,ow ya nama saya okama. saya masyarakat awam yang tertarik dengan tulisan-tulisan mu...salam kenal
ReplyDeleteKak gimana sih cara membuat truktur aspartat dan treonin saat kondisi lingkungan asam, isoelektrik, dan basa
ReplyDelete